Zelf leven van de grond af opbouwen. Uit niks meer dan losse moleculen. Scheikundigen proberen het, maar dat is nog niet makkelijk. In een reeks spoedcursussen praat Kennislink je snel bij over hoe je van een knutseldoos met moleculen tot iets kan komen dat op leven lijkt. Deze week: wat is katalyse?

De autokatalysator reinigt uitlaatgassen door roet helemaal te laten verbranden.
Wikimedia Commons, Ahanix1989 in publieke domeinHet aanrecht staat weer vol met afwas. Elke dag na het avondeten staan de aangekoekte pannen en vette borden je aan te kijken. Op zulke momenten zou je willen dat het vanzelf gaat. Dat je niet elke avond een half uur bezig bent met schrobben, maar dat de klus in een minuutje gepiept is. Wat zou het handig zijn om een stofje tussen de vaat te stoppen, waardoor de afwas klaar is in een oogwenk.
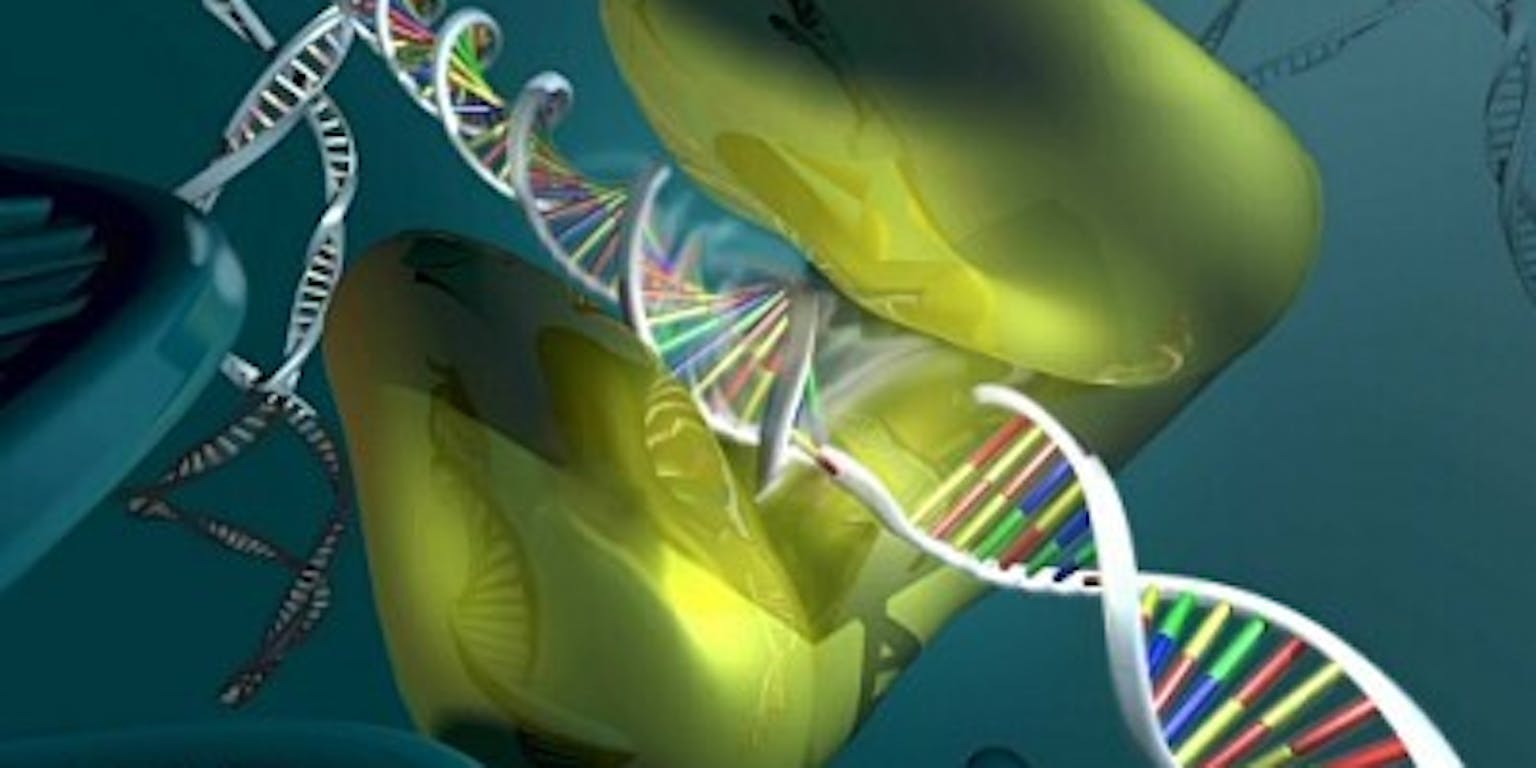
Zulke hulpstoffen bestaan, ze heten katalysatoren. Er zijn helaas (nog) geen handige katalysatoren die je de hele afwas uit handen nemen, al zitten ze al wel in afwasmiddel en vind je ze overal om je heen. De bekendste is misschien wel de autokatalysator. Die zorgt ervoor dat uitlaatgassen zoals roet helemaal verbranden tot CO2 en water. De temperatuur in de motor en de uitlaat van een auto is niet hoog genoeg om het roet helemaal te laten reageren.
Vroeger kwam dat roet daardoor gewoon in de lucht terecht. De autokatalysator, gemaakt van de metalen platina en palladium, zorgt ervoor dat de reactie bij lagere temperatuur gebeurt. Als een scheikundige reactie sneller of schoner verloopt dankzij een toegevoegde hulpstof heet dat katalyse. Het bijzondere is dat een katalysator een chemische reactie kan beïnvloeden zonder zelf verbruikt te worden.
Tegen een berg op fietsen
Veel reacties zouden zonder katalysator alleen bij heel hoge temperaturen plaatsvinden. Er is veel energie nodig om ze op gang te brengen, terwijl ze lekker gaan als ze eenmaal gestart zijn. Je kunt het vergelijken met een berg waartegen je op moet fietsen: als je over het topje bent, gaat het trappen vanzelf en roetsj je naar beneden naar het dorpje in het dal. Maar als de berg te hoog is, zal je nooit in dat dorpje aankomen, of pas na uren en uren trappen. Een katalysator neemt de top van de berg weg. Er is minder energie nodig om de reactie te starten, dus loopt de reactie ook bij een lagere temperatuur.
Eén manier waarop een katalysator die bergtop wegneemt, is door te koppelen aan de moleculen van één van de stoffen die moeten reageren (een uitgangsstof). Doordat de katalysator het molecuul ‘vasthoudt’, worden bepaalde bindingen in dat molecuul verzwakt, zodat ze gemakkelijker verbreken en dus nieuwe verbindingen kunnen aangaan met andere moleculen.

Ammoniak is de basis van moderne kunstmeststoffen.
Wikimedia Commons, Rasbak via CC BY-SA 3.0Kunstmest
Een voorbeeld. We maken ammoniak voor in kunstmest uit waterstof en stikstof met behulp van een ijzerkatalysator. De water- en stikstofmoleculen (H2 en N2) hechten aan het ijzer, dat ze uiteen laat vallen in losse atomen. Die losse atomen combineren zich vervolgens tot ammoniakmoleculen (NH3). De katalysator laat het molecuul los als het gereageerd heeft, zodat het weer opnieuw een van de uitgangsstoffen kan vastpakken. Zo kan hij doorwerken tot alle uitgangsstoffen opgebruikt zijn.
Enzymen
In de natuur wordt katalyse voortdurend gebruikt. In alle levende organismen komen katalysatoren voor. In mensen, dieren en planten maar ook in eencellige bacteriën. Meestal gaat het om eiwitten die het lichaam zelf maakt. Eiwitten die werken als katalysator noemen we enzymen. Een enzym is dus niets anders dan een biologische katalysator: een biologische stof die een reactie versnelt zonder zelf opgebruikt te worden.
Enzymen zijn essentieel: ze helpen bij het verteren van de maaltijd die je net gegeten hebt. Ze maken de energie vrij die in dat eten opgeslagen ligt zodat het gebruikt kan worden in de cellen van je lichaam. Ze helpen bij de groei en reparatie van weefsels, organen en cellen. Dankzij enzymen verlopen alle processen die nodig zijn voor leven efficiënt.

Enzymen helpen bijvoorbeeld bij het verteren van eten.
Beata GoreckaHelpen bij zelfassemblage
Ze werken vaak doordat ze verschillende moleculen binden die daardoor dicht genoeg bij elkaar komen om met elkaar te reageren. Dat is handig in de soep van allerhande stoffen waarin ze zich bevinden. Enzymen zijn kieskeurig: elk enzym bindt maar aan één of een paar specifieke moleculen.
Enzymen kunnen ook helpen bij de zelfassemblage van moleculen. Dat werkt als volgt. Enzymen binden aan specifieke moleculen en knippen er een stukje af. Zo zijn er enzymen die het uiteinde van losse eiwitten eraf knippen. De kleinere eiwitten die overblijven zijn in staat om spontaan aan elkaar te koppelen tot een lange keten. Op die manier worden allerlei structuren gevormd waaruit een levende cel bestaat.