Mihai Netea van het Radboudumc in Nijmegen is dit jaar één van de winnaars van de Spinozapremie. Hij ontdekte hoe het afweersysteem de gevaarlijke schimmel Candida albicans herkent. Die kennis moet in de toekomst leiden tot betere behandelingen tegen infecties. NEMO Kennislink sprak Netea over zijn passie voor het afweersysteem.
De schimmel Candida albicans komt van nature voor op het menselijk lichaam. Meestal zonder klachten te veroorzaken. Maar soms zorgt de schimmel voor plaatselijke infecties, zoals op de huid of de slijmvliezen van de vagina. Bij mensen met een sterk verminderde afweer (bijvoorbeeld door ziekte of na een operatie) kan Candida albicans in het bloed terecht komen, met een levensgevaarlijke bloedvergiftiging tot gevolg. Mihai Netea, hoogleraar Experimentele Interne Geneeskunde in het Radboudumc, doet onderzoek aan deze schimmel en de relatie met het afweersysteem.

Mihai Netea, hoogleraar Experimentele Interne Geneeskunde in het Radboudumc.
Academy of EuropeZomerschool
“Het is grappig hoe dat gaat”, antwoordt Netea op de vraag waar zijn interesse voor afweerreacties vandaan komt. “Begin jaren tachtig las ik een onderzoek over het gebruik van interleukine-2 (een signaalstof, gemaakt door afweercellen) bij kanker. Ik was student en woonde in Roemenië, maar ik had meteen zoiets van ‘daar moet ik wat mee doen!’ Het onderzoek naar signaalstoffen van het afweersysteem stond toen nog echt aan het begin.”
Netea volgde een zomerschool immunologie in Amsterdam en kwam daar hoogleraar Jos van der Meer tegen. “Hij is mijn mentor geworden. Ik werkte enkele zomers mee in zijn lab en kwam uiteindelijk naar Nederland om onderzoek te kunnen doen.”
Aangeboren afweer omhoog
Dat onderzoek richtte zich al snel op de afweerreactie tegen schimmels, want daarover was nog veel minder bekend dan over bacteriële infecties. “Ik beschreef hoe onze eerste afweerreactie (de aangeboren afweer) Candida albicans herkent en welke receptoren daarvoor nodig zijn”, vertelt Netea. “Vervolgens ben ik gaan kijken welke mechanismen zijn gestoord in patiënten die erg gevoelig zijn voor infecties.”
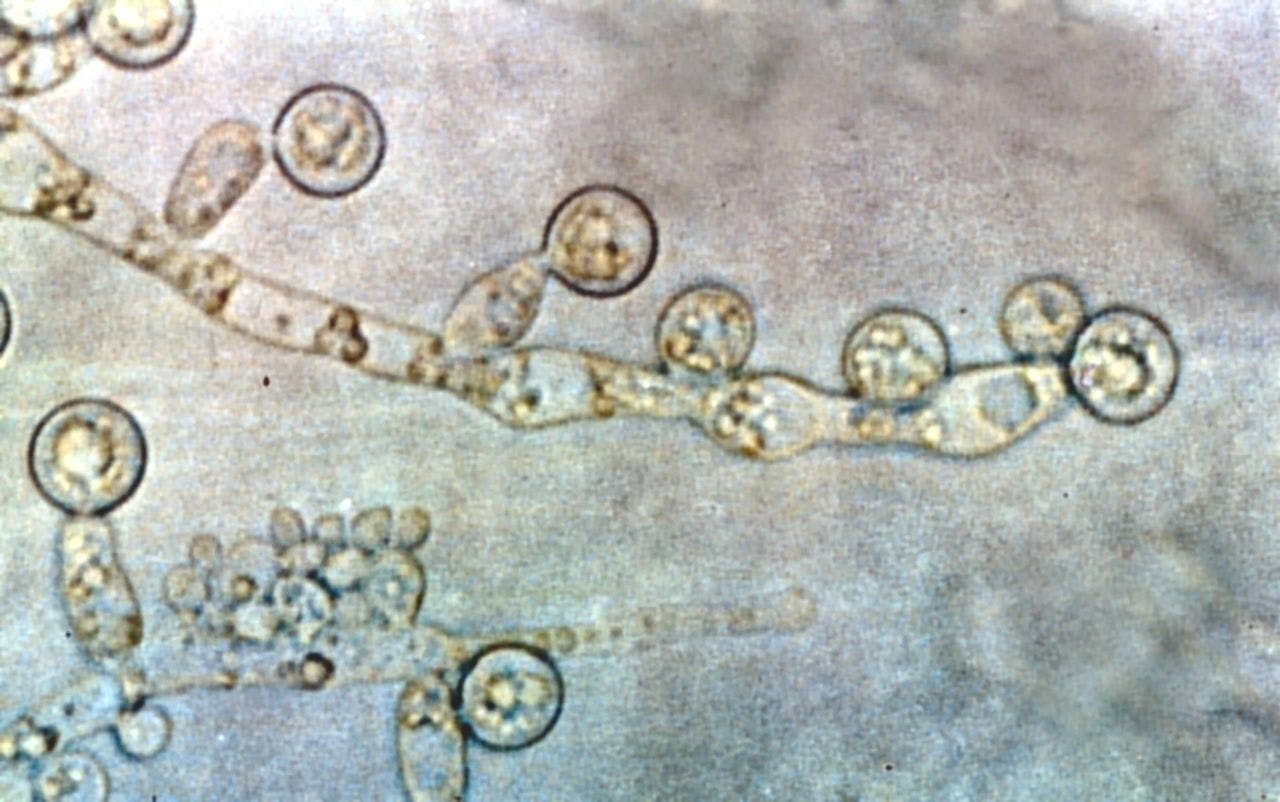
De schimmel Candida albicans komt van nature voor op het menselijk lichaam. Meestal zonder klachten te veroorzaken. Maar soms zorgt de schimmel voor plaatselijke infecties, zoals op de huid of de slijmvliezen van de vagina.
GrahamColm - Own work, via CC BY-SA 3.0“Toen ontdekte ik iets bijzonders. Namelijk dat de aangeboren afweer verandert na een schimmelinfectie (en trouwens ook na bacteriële infecties). De aangeboren afweer wordt, als het ware, wat hoger gezet en er ontstaat een geheugen dat zorgt voor een verbeterde afweer tegen een volgende infectie.” Dit aanpassen van de afweerreactie was voorheen alleen bekend van de gespecialiseerde, adaptieve afweer. De huidige vaccins zijn gebaseerd op het idee dat de adaptieve afweer kan leren om een ziekteverwekker te herkennen en vroegtijdig in te grijpen. De aangeboren afweer heeft dat lerend vermogen ook en dat wil Netea gaan gebruiken om vaccins te verbeteren.
Goede kant van het verhaal
De Spinozapremie komt daarbij goed van pas. De immunoloog vindt het fantastisch dat zijn werk zo’n belangrijke onderscheiding verdient. “Ik was op een conferentie in Amerika toen ik een telefoontje kreeg uit Nederland”, vertelt hij enthousiast. “Ik had geen idee wie dat zou kunnen zijn, maar toen ik hoorde waar het over ging was ik heel blij. Ik vind het een grote eer en het geeft mogelijkheden voor vervolgonderzoek.”
Dat vervolgonderzoek richt zich dus met name op het verbeteren van vaccins. Door zowel het lerend vermogen van de adaptieve afweer als dat van de aangeboren afweer te gebruiken worden vaccins krachtiger, verwacht Netea. “Dat is de goede kant van het verhaal. Maar de aangeboren afweer kan ook weleens verkeerd reageren; op de verkeerde tijd of de verkeerde plek. Ontstekingen of een auto-immuunziekte kunnen dan het gevolg zijn. Wij hebben initiële aannames dat dit bijvoorbeeld zo is bij atherosclerose. In dat geval zou je de aangeboren afweer juist willen remmen.”

