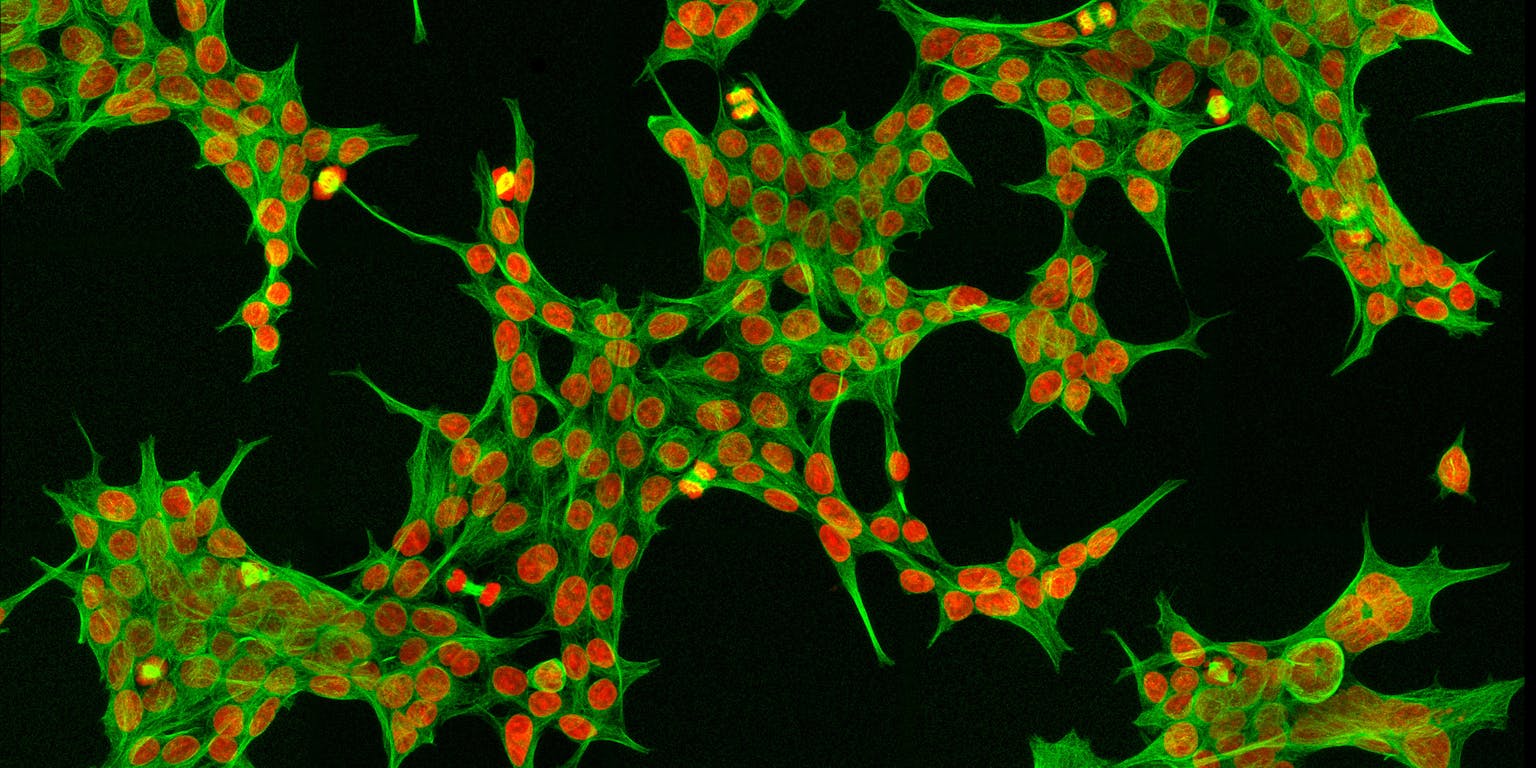
De Leidse hoogleraar Lex van der Eb ontwikkelde in de jaren zeventig de eerste Nederlandse cellijn. Dankzij de techniek erachter zijn al tientallen vaccins gemaakt. Hoe kwam die cellijn tot stand?
Het begon met één enkele cel in een reageerbuisje. Dat werden er twee. Een dag later hadden deze zich verdubbeld. Nog eens 24 uur later opnieuw. De cellen moesten over meerdere buizen verdeeld worden. Ze bleven groeien zolang ze de ruimte kregen. Het was 1973 en de onsterfelijke cellijn HEK-293 was geboren.
Dankzij de techniek die hieraan ten grondslag ligt, is er nu een vaccin tegen ebola. Tegen zikavirus, griep en corona. Zijn er tientallen wetenschappelijke ontdekkingen gedaan. Maar dat kon Lex van der Eb allemaal nog niet voorzien toen hij in 1970 met zijn onderzoek begon. Zijn doel was destijds om het ontstaan van kanker beter te begrijpen. Waarom verandert een gezonde menselijke cel in een kankercel?
Hij gebruikte voor zijn onderzoek een voor de mens onschuldig verkoudheidsvirus. Als dit virus de cellen van zijn gastheer infecteert, dwingt het de gastheercellen tot het maken van kopieën van het virus-DNA - iets wat een virus zelf niet kan omdat het geen stofwisseling heeft. De gastheercellen gaan daardoor dood en het nakomelingsvirus kan zich verspreiden.
Maar als rattencellen in het lab met het DNA uit het virus worden geïnfecteerd, kan zich ook een ander scenario voltrekken. In dat scenario integreert de gezonde cel het virus-DNA in het eigen DNA en gaat zo ongebreideld delen. Hij wordt tumorcel. De ideale manier om het ontstaan van kanker te onderzoeken, leek Van der Eb.
Om de gezonde cel binnen te dringen, gebruikt het virus een soort jasje van eiwitten, maar Van der Eb wilde virus-DNA zonder eiwitten een rattencel in laten gaan. “Dat was gemakkelijker gezegd dan gedaan”, schrijft zijn vrouw Titia van der Eb. “Het gezuiverde DNA maken was het probleem niet. Dat DNA ging alleen de cel niet in, wat Lex en zijn post-doc student Frank Graham ook deden.”

De Leidse hoogleraar Lex van der Eb
Taco van der EbMoreel belastend
Na twee jaar en honderden experimenten verder wilden ze er bijna mee stoppen. Maar Graham wilde nog één ding proberen. “Frank had gelezen dat bacteriën calciumchloride gebruiken om vreemd DNA in hun cellen op te nemen, dus hij voegde dat toe aan het kweekmedium (de vloeistof die gebruikt wordt om cellen te voeden, red.).” Tot hun grote verbazing werkte het. “Er ontstond een neerslag van calciumfosfaat waarin het DNA gevangen zat. Dat ging aan de cellen kleven en een deel ging daadwerkelijk de cel in.” De calciumfosfaattechniek was geboren. Een techniek die nu nog steeds gebruikt wordt om DNA cellen in te brengen.
De onderzoekers waren dolenthousiast, vertelt Van der Eb. “En het gaf hun de stimulans om door te gaan. Want het was nu weliswaar gelukt met rattencellen, maar nog niet met menselijke cellen.” Zou het ook lukken om menselijke cellen te manipuleren met het DNA van verkoudheidsvirussen? Om die te veranderen in een eeuwig delende, onsterfelijke cellijn: een groep identieke cellen die oneindig in leven zou blijven en die van grote waarde zou zijn voor het (kanker)onderzoek?
Een paar deuren verder, in het Academisch Ziekenhuis Leiden - de voorganger van het Leids Universitair Medisch Centrum - koos een vrouw voor abortus. Zij besloot de foetus af te staan aan de wetenschap. “Destijds ging die toestemming nog mondeling en in wederzijds vertrouwen”, schrijft Van der Eb. De wettelijke richtlijnen voor foetaal weefsel kwamen pas in 2002. “De medische gegevens van de zwangerschapsafbreking en het patiëntendossier zijn gewist waardoor de privacy van de moeder gewaarborgd bleef.”
Lex van der Eb kreeg de foetus voor zijn onderzoek en zag dit als een enorme kans. “Foetale cellen zijn jonge, goed delende cellen en er is minder kans dat zij al besmet zijn met bacteriën of virussen.” Hij voerde het onderzoek zelf uit. “Het opereren van een foetus moet met alle respect en eerbied worden gedaan. Vanwege de morele belasting wilde hij die zware verantwoordelijkheid niet bij zijn jonge collega’s neerleggen.” De onderzoeker haalde niercellen uit de foetus en voegde met behulp van de calciumfosfaattechniek verkoudheidsvirus toe. Na een groot aantal experimenten ontstond één klompje getransformeerde cellen die de onderzoekers konden doorkweken.
Veldbed in het lab
En zo was de HEK-293 cellijn geboren: humane embryonale niercel 293. Het getal 293 is het experimentnummer en verraadt het aantal pogingen dat nodig was om de cellijn te maken.
Om die cellijn in leven te houden bestond destijds nog geen apparatuur. “Alles ging met de hand. Lex sliep in die begindagen op een veldbed in het lab met een wekker naast zich. Om de paar uur moest hij de cellen pipetteren naar nieuwe buisjes. Soms ging ik mee om te helpen de buisjes te schudden.”
Lex van der Eb vindt het belangrijk om te benadrukken dat hij toen nog helemaal geen toepassingen in zijn hoofd had en niet kon vermoeden wat er later allemaal met de cellen zou gebeuren. “Hij was alleen maar heel nieuwsgierig”, schrijft zijn vrouw. “Tegenwoordig moet onderzoek doelgericht zijn en snel resultaat opleveren. Hij heeft geluk gehad dat hij de kans kreeg om fundamenteel onderzoek uit te voeren en zo lang te proberen.”
Niet levensvatbaar
Het was een oud-promovendus van Van der Eb, Dinko Valerio, die over klinische toepassingen van de Leidse cellijn begon. Daarvoor was wel een nieuwe, verbeterde versie nodig die voldeed aan de strenge farmaceutische standaarden, zoals een nauwkeurige donorgeschiedenis. Omdat de medische gegevens van de donor van de niercellen niet bewaard waren gebleven, was de HEK-293-cellijn destijds ongeschikt voor commerciële toepassingen.
En zo ontstond uiteindelijk de onsterfelijke cellijn PER.C6 (primary embryonic retina clone 6), gemaakt uit één enkele netvliescel die getransformeerd was naar een eeuwig delende cel. Die netvliescel kwam van een niet-levensvatbare foetus die in 1985 werd geaborteerd. “De ouders gaven na afloop van de abortus toestemming voor gebruik van de foetus voor onderzoeksdoeleinden. De naam van de donor werd niet bekendgemaakt en haar gegevens zijn na een aantal jaar vernietigd.”
PER.C6 is te kweken in tanks van tienduizend liter waarmee op grote schaal bestanddelen voor vaccins worden gemaakt. Ideaal voor de farmaceutische industrie. Dat blijkt ook uit het feit dat farmareus Johnson & Johnson in 2011 Janssen Vaccins kocht, dat eerder al Valerio’s bedrijf Crucell overnam. Zo kwamen de cellen in Amerikaanse handen. In 2021 kwam Johnson & Johnson met een coronavaccin gemaakt met PER.C6 cellen. De technologie is gepatenteerd en wordt onder licentie aan andere bedrijven verkocht.
De HEK-cellen zijn nog altijd vrij verkrijgbaar en niet-gepatenteerd. En ondanks dat ze eerder niet geschikt leken voor de farmaceutische industrie, worden ze over heel de wereld gebruikt. Alleen al tijdens de coronapandemie. Zowel voor het Pfizer-, het AstraZeneca-, het Russische Sputnik- en het Moderna-vaccin zijn HEK-cellen gebruikt.
Twee kinderen die nooit ter wereld kwamen, zorgden ervoor dat miljoenen mensen met vaccins zijn geholpen. Van der Eb: “Dat is toch mooi?”