Planten gebruiken zonlicht als energiebron. Ze kunnen fotonen (licht) heel efficiënt omzetten in elektronen die vervolgens worden gebruikt in chemische reacties. Maar verrassend genoeg verloopt het transport van die elektronen nogal chaotisch, zo ontdekten onderzoekers van de Rijksuniversiteit Groningen door simulaties van een belangrijk eiwitcomplex.
Planten en sommige bacteriën gebruiken een groot eiwitcomplex, fotosysteem II (FSII), om fotonen (licht) om te zetten in vrije elektronen. Het molecuul plastochinon brengt dan de vrije elektronen naar de volgende stap in de keten die uiteindelijk zorgt voor de productie van ATP, de universele energiedrager van levende cellen. Dit staat allemaal in de leerboeken biologie en over de verschillende onderdelen van het systeem is inmiddels heel veel bekend. Maar nog onbekend was hoe plastochinon het FSII complex binnenkomt om de elektronen op te halen en het weer verlaat om zijn belangrijke transportwerk te verrichten.
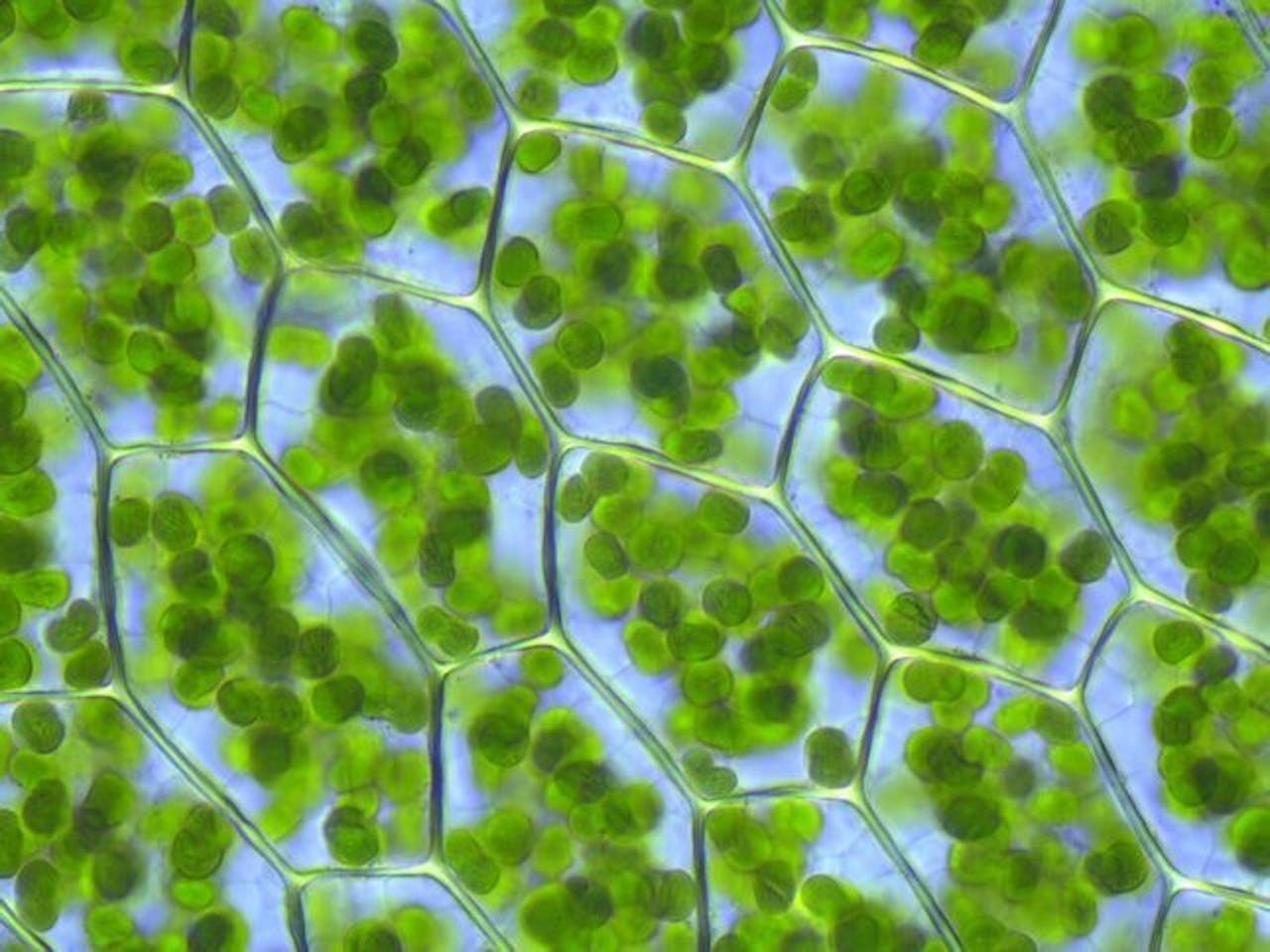
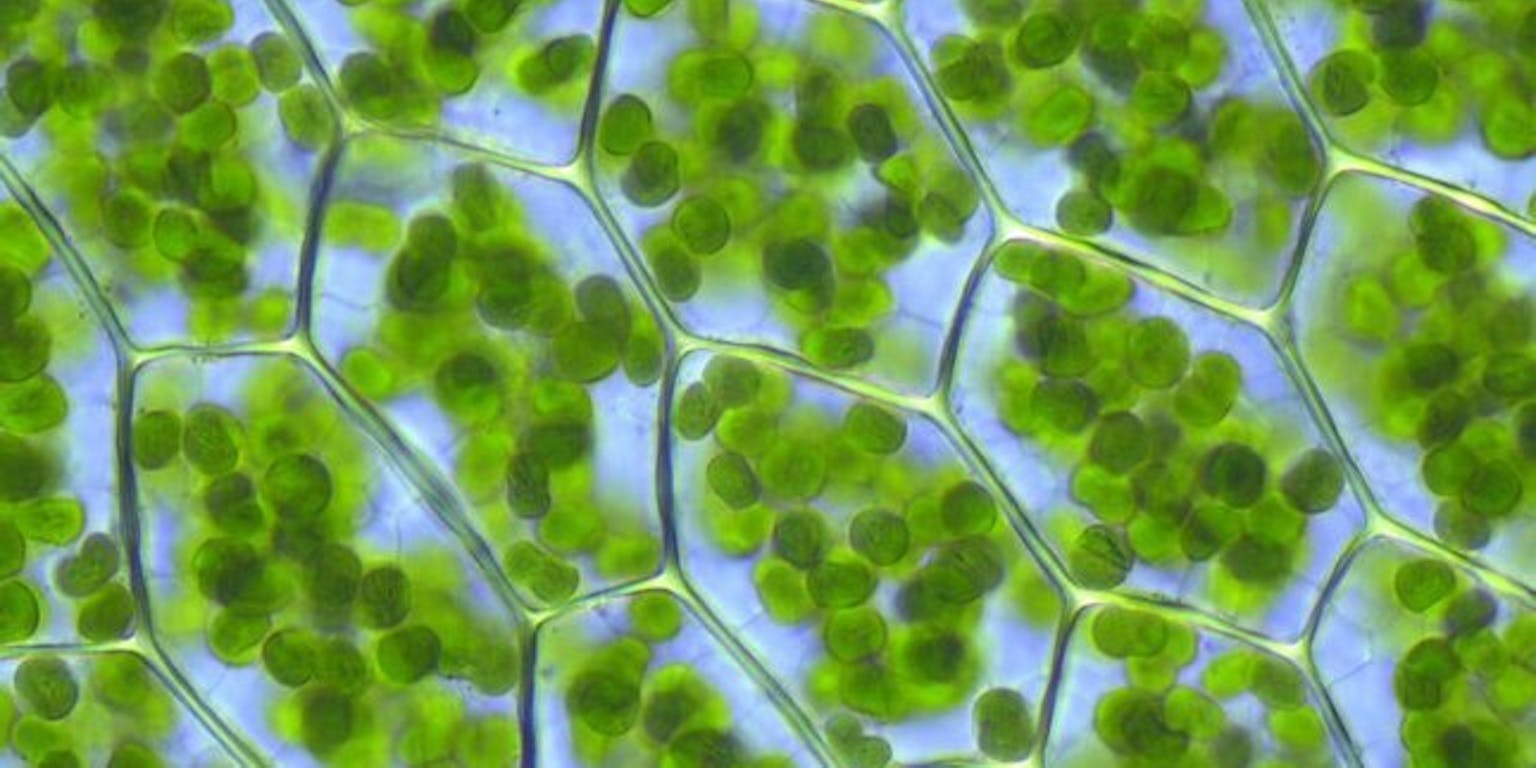
Bladgroenkorrels in rond boogsterrenmos, Plagiomnium affine. De bladgroenkorrels of chloroplasten vangen het zonlicht op, waardoor de fotosynthese van start kan. Het fotosysteem II (FSII) bevindt zich in de bladgroenkorrels.
Kristian Peters via Wikimedia Commons CC BY-SA 3.0“De structuur van FSII is al bekend en op basis van het statische plaatje was af te leiden dat er twee kanalen zijn waardoor plastochinon naar binnen en weer naar buiten kan”, zegt Siewert-Jan Marrink, hoogleraar Moleculaire Dynamica van de Rijksuniversiteit Groningen. “Maar zo simpel is het dus niet.”
Marrink, zijn promovendus Floris van Eerden en nog enkele collega’s gebruikten moleculaire dynamica om de interactie van FSII met plastochinon te bestuderen. Ze publiceerden hun resultaten in het tijdschrift Nature Communications. Moleculaire dynamica draait kort gezegd om het simuleren van het gedrag en de beweging van moleculen via computermodellen. Daarvoor moesten ze het enorme FSII complex, dat bestaat uit verschillende eiwitten en andere moleculen, modelleren. Een groot computercluster was nodig om de interactie tussen de verschillende onderdelen van FSII uit te rekenen.
Blok beton
Floris van Eerden deed het meeste modelleerwerk. “Het kostte ongeveer twee jaar om alles aan de praat te krijgen”, legt hij uit. Hij modelleerde niet alleen het complex, maar ook de lipide-membraan, het omhulsel, van de bladgroenkorrels in de bladeren waar het zich normaal gesproken in bevindt. De eerste resultaten waren niet veelbelovend. “FSII is erg stabiel, het leek wel een blok beton”, zegt Van Eerden. Maar toen hij meer in detail ging kijken zag hij meer dynamiek – vooral de plastochinon moleculen bleken erg beweeglijk. “Het plastichinon zonder extra elektronen ging inderdaad het FSII complex in en bond zich in een ‘uitwisselingsholte’. Nadat het hier de elektronen had opgepikt, liet het plastochinon weer los en verliet het FSII.”
&feature=youtu.be
Een verrassing was de ongecontroleerde manier waarop dit allemaal plaatsvond. “Het idee dat iedereen had, was dat er twee kanalen waren waar plastochinon doorheen ging. Eentje om naar binnen te gaan en eentje om weer naar buiten te gaan”, vertelt Marrink. Maar er bleken drie kanalen te zijn die allemaal werden gebruikt om zowel naar binnen als naar buiten te gaan. “De natuur bleek niet zo geordend als we hadden gedacht.” Wanneer een plastochinon molecuul eenmaal in de membraan zat, ging het al snel het FSII complex binnen. Maar het kwam er soms direct weer uit, zonder elektronen, of het bleef een tijdje in het complex ronddobberen voordat het eindelijk bond in de uitwisselingsholte en daar dan elektronen ontving. Marrink: “Toevallige beweging lijkt alles te bepalen.”
Toch is het hele proces van het omzetten van een opgevangen foton in een elektron, extreem efficiënt. Veel efficiënter dan door mensen gebouwde zonnepanelen. Misschien dat er dus iets te leren valt van de natuur. En de landbouw zou op termijn ook zijn voordeel kunnen doen met deze nieuwe kennis over de werking van FSII. “Er zijn nogal wat onkruidbestrijdingsmiddelen die op dit systeem aangrijpen”, zegt Van Eerden. Maar uiteindelijk is het toch vooral het uitpluizen van de indrukwekkende complexiteit van het systeem waar de wetenschappers blij van worden. “Dat is echt ongelooflijk”, verzucht Marrink.