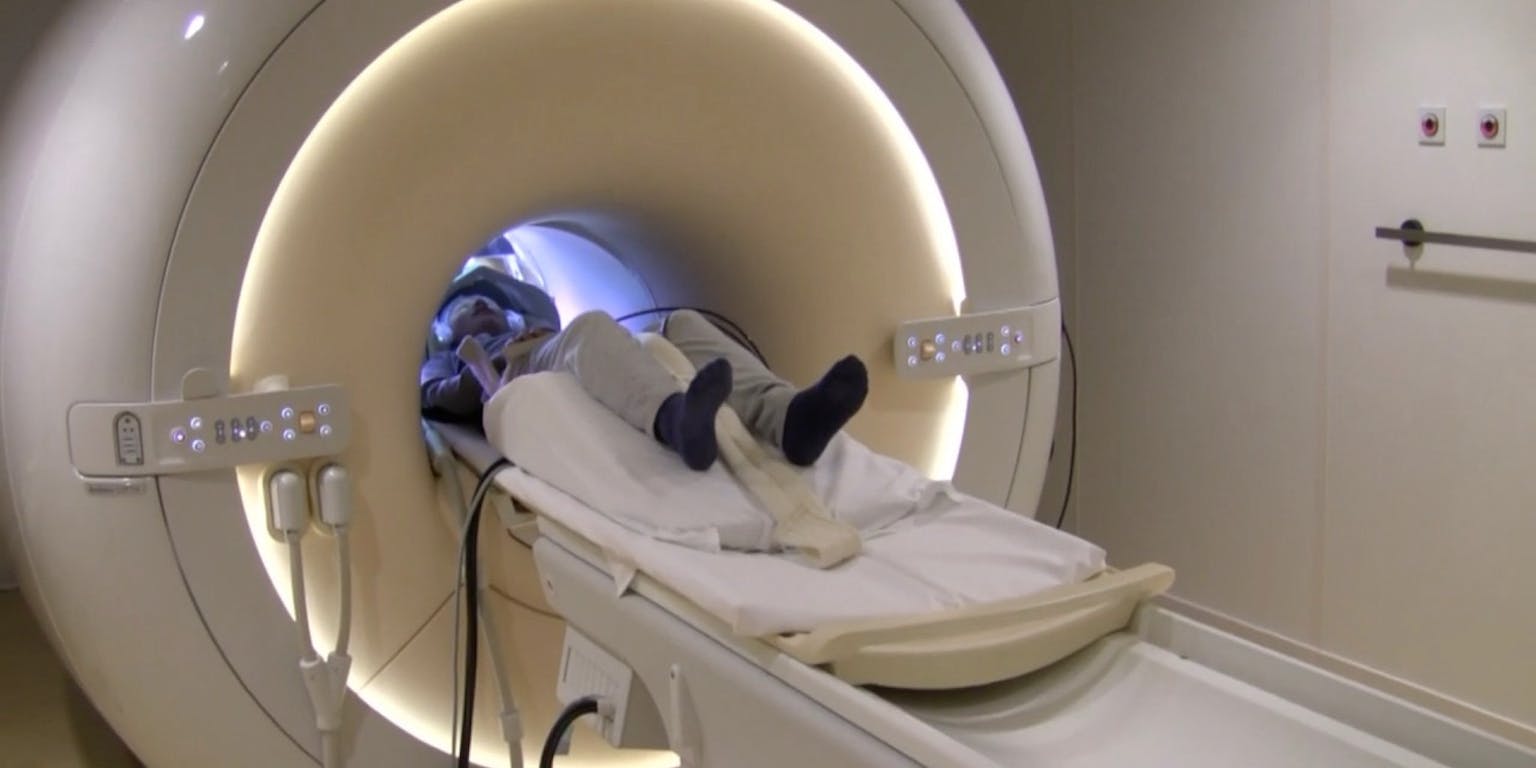
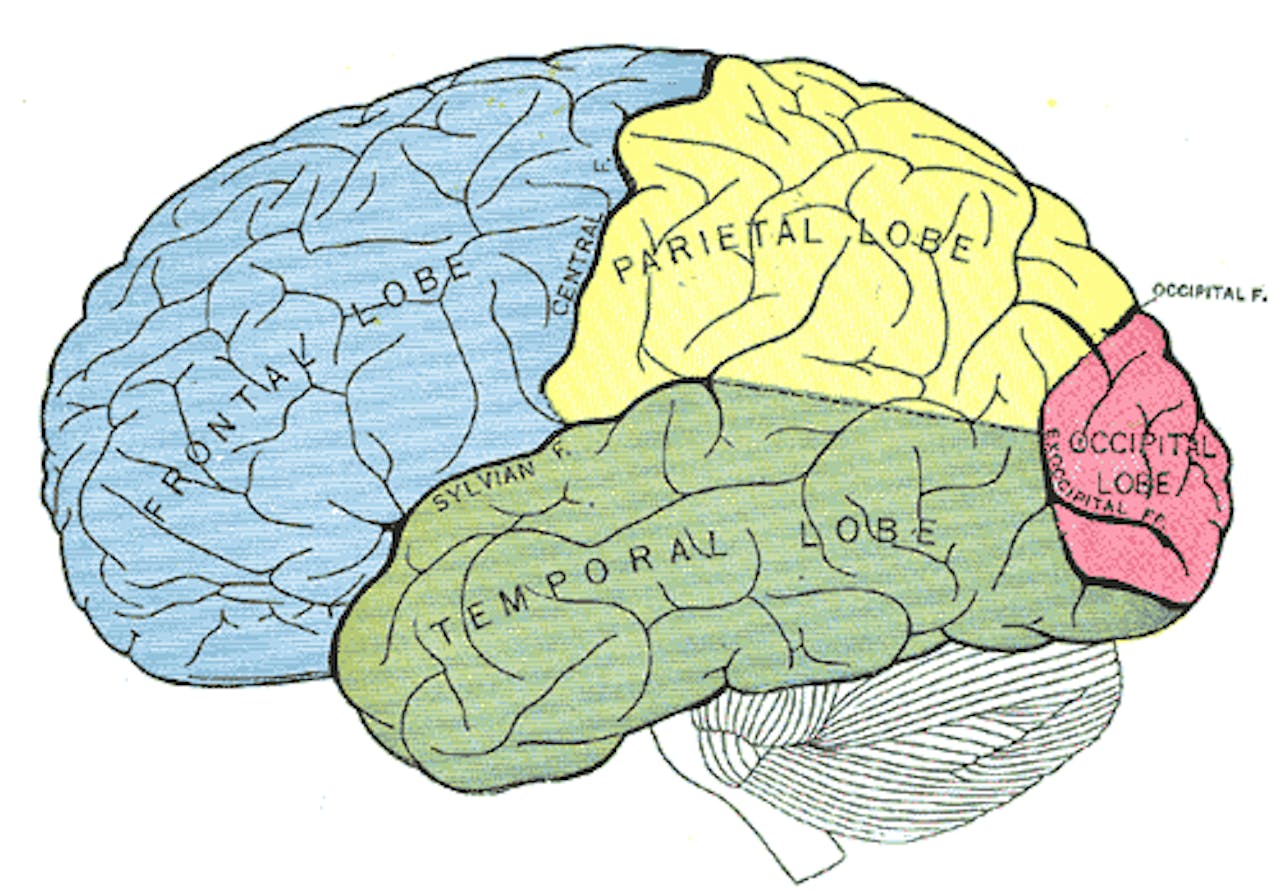
Jaren voordat mensen met een erfelijke vorm van frontotemporale dementie klachten krijgen, beginnen hun hersenen en cognitieve vaardigheden al te veranderen. Neurowetenschapper Lize Jiskoot bracht het ziekteproces in beeld.
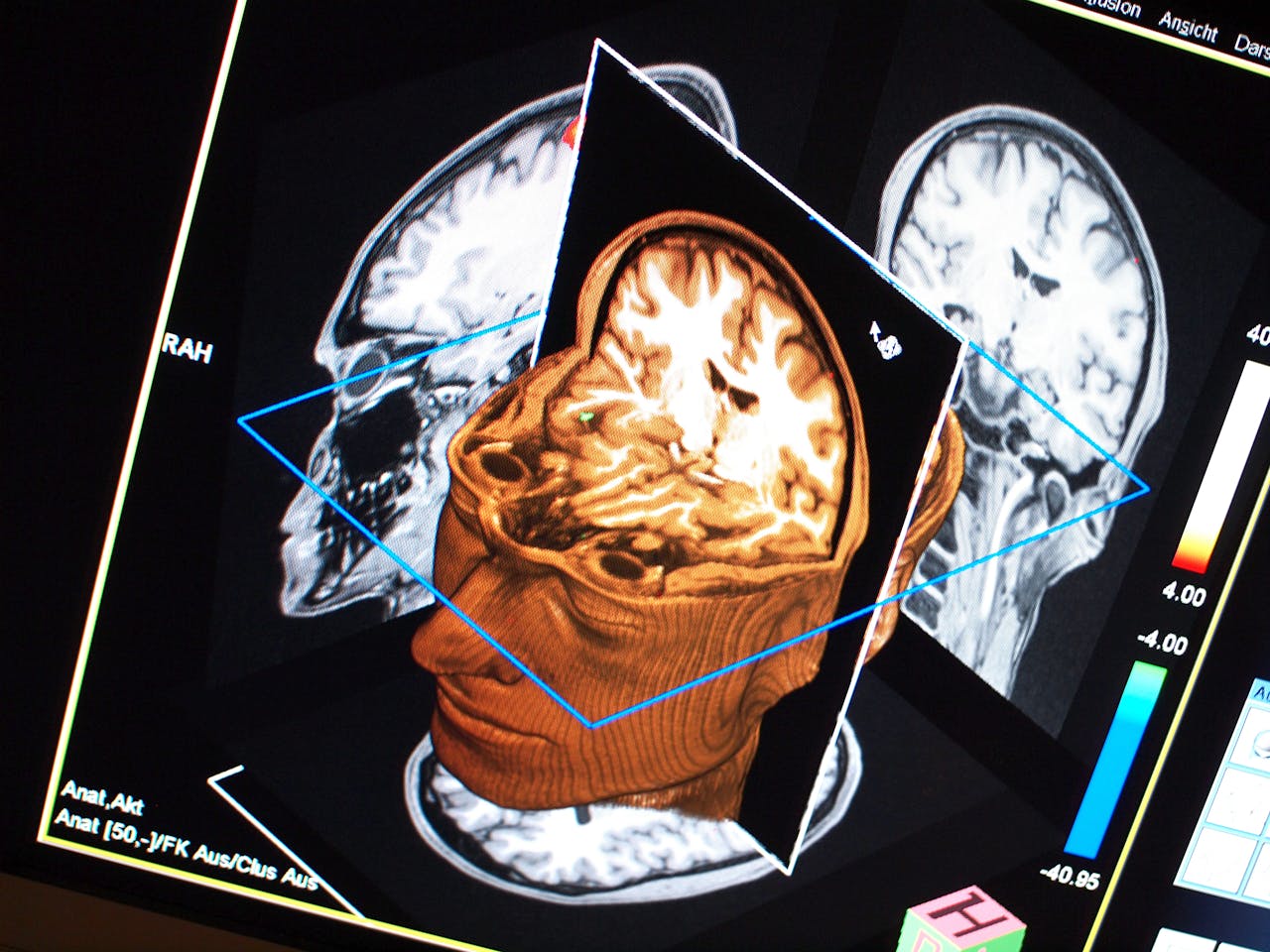
Al jaren voor symptomen van dementie ontstaan, zijn er veranderingen te zien in de hersenen.
Flickr.com, Ars Electronica via CC BY-NC-ND 2.0Dementie behandelen is lastig; een medicijn is er niet. Eigenlijk moeten we de ziekte voor zijn. Wetenschappers zoeken dan ook naar manieren om de hersenschade op te ruimen voordat je er last van krijgt. Van de ziekte van Alzheimer weten we namelijk dat eiwitten zich in de hersenen ophopen, al vijftien jaar voor de eerste symptomen optreden. Pas jaren later beginnen zenuwcellen (de grijze massa) daadwerkelijk af te sterven.
Voor frontotemporale dementie (FTD), de vorm van dementie die het vaakst voorkomt bij mensen jonger dan 65, kennen we het ziekteverloop minder goed. Reden voor klinisch neurowetenschapper Lize Jiskoot om te zoeken naar meetbare kenmerken (biomarkers) die iets vertellen over het stadium en het verloop van de ziekte.
“We wisten al dat bij patiënten met FTD de witte stof in de hersenen, die bestaat uit de uitlopers van zenuwcellen, is aangetast”, legt Jiskoot uit. Tijdens haar promotieondezoek aan de Erasmus Universiteit Rotterdam keek ze naar mensen met een erfelijke vorm van FTD. Bij hen begint de witte stof al jaren voordat zij de eerste klachten krijgen af te wijken. Jiskoot: “We zijn op het punt dat we hiermee kunnen voorspellen dat de ziekte eraan komt.”
DNA-mutatie
Net zoals bij Alzheimer bestaat er van frontotemporale dementie een spontane variant en een erfelijke vorm. Jiskoot richtte zich op die laatste groep. “Wie een ouder heeft met FTD, heeft vijftig procent kans de ziekte zelf ook te krijgen.” Er zijn drie grote DNA-mutaties bekend die allemaal op zichzelf leiden tot een vorm van FTD. Als je zo’n mutatie erft is het vrij zeker dat je FTD gaat ontwikkelen. Niet iedereen krijgt dezelfde symptomen. Afhankelijk van het type mutatie krijgen sommige patiënten gedragsproblemen, terwijl bij anderen taalproblemen meer op de voorgrond staan. Soms gaat FTD samen met de ziekte ALS (amyotrofische lateraalsclerose); dan komen er ook nog problemen met spierbewegingen bij.
De afgelopen zes jaar werkte Jiskoot, naast haar promotieonderzoek, als neuropsycholoog in het Alzheimercentrum Erasmus MC. Ze zag veel mensen met FTD, bij wie ze een neuropsychologisch onderzoek deed. Daarbij breng je de klachten in kaart en meet je met testen de cognitieve functies, zoals geheugen, aandacht en taalvaardigheid (lezen en schrijven).
Sinds 2010 volgen de Rotterdammers een groep mensen die een FTD-mutatie bij zich dragen, maar nog geen symptomen hebben. Eens per twee jaar komen deze mensen naar het Erasmus MC, waar Jiskoot en haar collega’s cognitieve tests afnamen en hersenscans maken. Jiskoot: “We willen de eerste veranderingen in zowel de hersenen als cognitie en gedrag oppikken.”
Probleem van de witte stof
Met een gewone MRI-scan maakten de onderzoekers opnames van de hersenstructuur. Daarnaast gebruikten ze nog een speciale MRI-techniek: diffusion tensor imaging. Hiermee is de kwaliteit van de witte stof te meten, ook al is die voor het blote oog ogenschijnlijk nog intact.
“We zagen dat de witte stof van mindere kwaliteit is bij mensen met de mutatie”, aldus Jiskoot. De witte stof bestaat uit de uitlopers van zenuwcellen. Elektrische signalen reizen via deze uitlopers van cel naar cel. De goede geleiding komt door een isolerend stofje met een witte kleur dat om de uitlopers ligt, genaamd myeline. Bij mutatiedragers geleiden de elektrische signalen minder goed dan bij mensen zonder mutatie.
Jiskoot: “Waar Alzheimer van oudsher een ziekte is van de grijze stof, raken we er steeds meer van overtuigd dat FTD toch meer een witte-stof-probleem is, zeker in het begin van de ziekte.” Verlies van de grijze stof volgt later en lijkt minder omvangrijk dan de aantasting van de witte stof.
Cognitieve achteruitgang
Ook met neuropsychologisch onderzoek volg je goed hoe de ziekte zich ontwikkelt, concludeert Jiskoot in haar proefschrift. “Stel dat je normaal vijftig punten scoort op een cognitieve test. Tien jaar later scoor je nog maar veertig punten, terwijl mensen zonder mutatie even goed blijven presteren. Dat wijst erop dat de fase zonder klachten overgaat in de fase met symptomen. Op zo’n moment kan je in principe nog klachtenvrij zijn, maar het onderliggende ziekteproces is wel begonnen.”
Overigens zijn de cognitieve verschillen tussen mensen met en zonder mutatie alleen zichtbaar op groepsniveau. Jiskoot: “Als je hun individuele score bekijkt zal je niet echt afwijkingen vinden. Je ziet het niet als iemand voor je staat.”
Wetenschappers hopen medicijnen te ontwikkelen die hersenschade opruimen voor mensen symptomen van dementie krijgen.
Wikimedia Commons CC BY-SA 3.0Van begin tot eind
Dankzij een grote internationale studie waar het Erasmus MC zich in 2012 bij aansloot, had Jiskoot toegang tot een grote stapel patiëntgegevens. Momenteel doen 24 onderzoekscentra in verschillende landen dezelfde MRI-scans en cognitieve tests bij in totaal achthonderd mutatiedragers. Daarvan komen er tweehonderd uit Nederland.
Gezamenlijk wist de internationale groep het ziekteverloop van begin tot eind te meten.
Grofweg ziet het plaatje er als volgt uit: dertig jaar van tevoren vermindert de kwaliteit van de witte stof. Tien jaar voor de eerste symptomen verschijnen gaat de grijze stof achteruit. Vijf jaar daarna zet vervolgens de cognitieve achteruitgang in.
Jiskoot denkt dat meer inzicht in het ziekteverloop de ontwikkeling van medicijnen gaat helpen. “Het is belangrijk dat we al vroeg onderscheid kunnen maken tussen Alzheimer en FTD, of tussen verschillende vormen van FTD. Als patiënten met dementie niet in de juiste terechtkomen, wordt het erg lastig om de werking van een geneesmiddel te testen.”