Nederlandse onderzoekers brachten in kaart hoe antilichamen een van de ‘opruimdiensten’ van ons lichaam activeren. Deze week beschrijven ze in Science hoe een ‘docking station’ van zes antilichamen daarbij een sleutelrol speelt. De moleculaire details zetten hen op het spoor van nieuwe therapeutische antilichamen voor effectieve immuuntherapie tegen kanker.
Voor een aantal soorten kanker, zoals borstkanker en leukemie, is al immuuntherapie beschikbaar. Dat werkt via therapeutische antilichamen die specifiek aan tumorcellen binden. Ze zijn als de stippen op de bomen in het bos: dit exemplaar is ziek, deze boom moet om.
Dankzij de moleculaire ‘stip’ van de therapeutische antilichamen ziet het afweersysteem van de patiënt dat een kankercel schadelijk is. Vervolgens komt één van de ‘opruimdiensten’ in actie, het zogenaamde complementsysteem, dat de cel onschadelijk maakt.
Het principe is makkelijk beschreven, maar aan de uitvoering zitten de nodige haken en ogen. Zo hebben nog niet alle kankerpatiënten baat bij immuuntherapie. Om daar verandering in te kunnen brengen willen wetenschappers precies weten hoe de therapeutische antilichamen hun werk doen. De focus ligt daarbij op het activeren van de opruimdienst.
Moleculaire interactie
“We weten al decennia dat het complementsysteem van groot belang is”, zegt Piet Gros, hoogleraar Biomacromoleculaire Kristallografie aan de Universiteit Utrecht. “Maar hoe het precies werkt niet. Daarom willen we meer weten over de moleculaire interactie tussen de antilichamen en het complementsysteem.”
Gros is één van de onderzoekers in een gezamenlijk onderzoeksproject van de Universiteit Utrecht, het Leids Universitair Medisch Centrum en het bedrijf Genmab, dat in Utrecht een belangrijk onderzoekslab heeft.
Aan de publicatie in Science heeft ook het Netherlands Centre for Nanoscopy (NeCEN) in Leiden een belangrijk aandeel. Gros’ promovendus Christoph Diebolder deed er onderzoek naar de antilichamen met een cryoTEM. Van deze zeer geavanceerde elektronenmicroscoop zijn wereldwijd slechts enkele apparaten beschikbaar voor universitair wetenschappelijk onderzoek.
Docking station
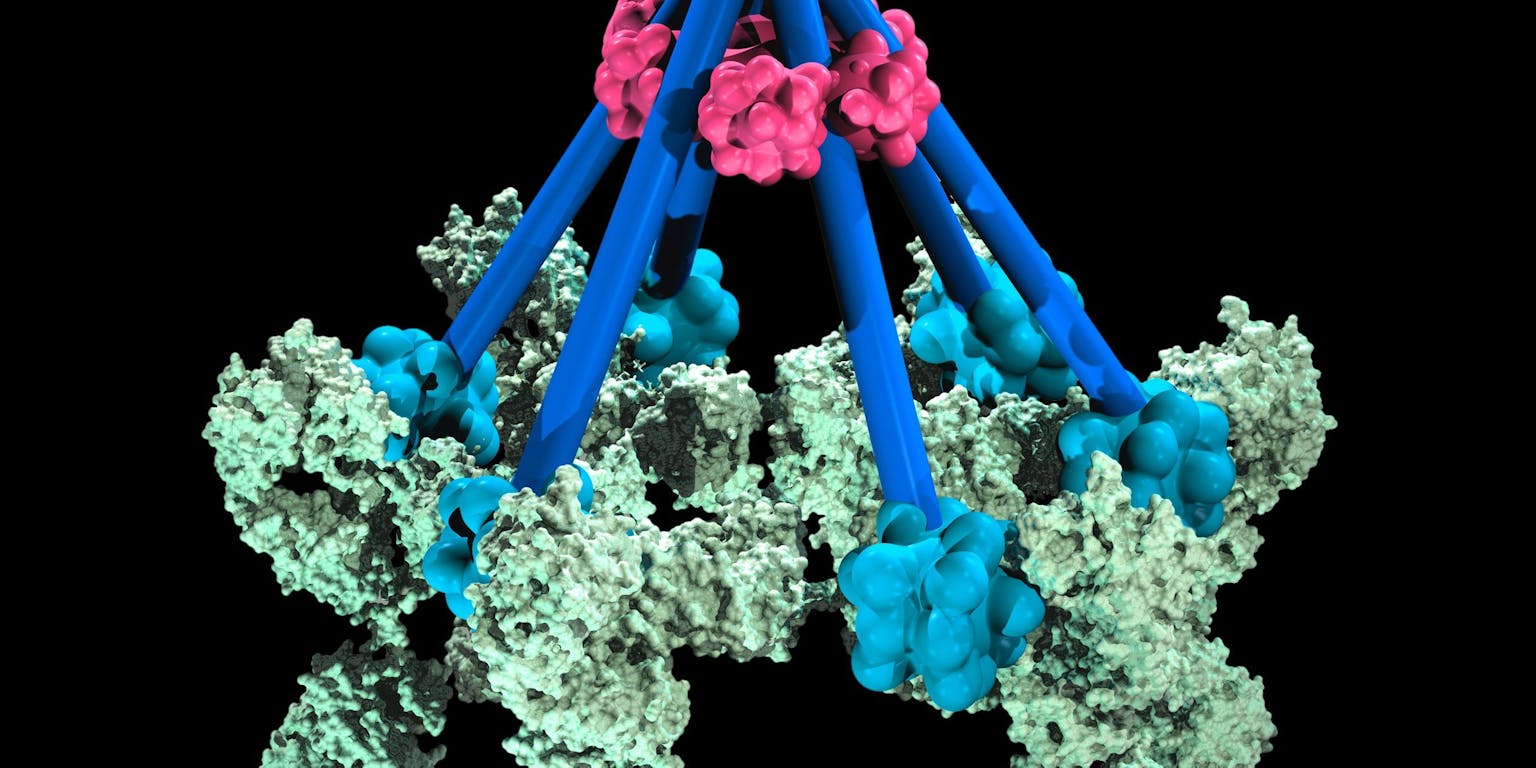
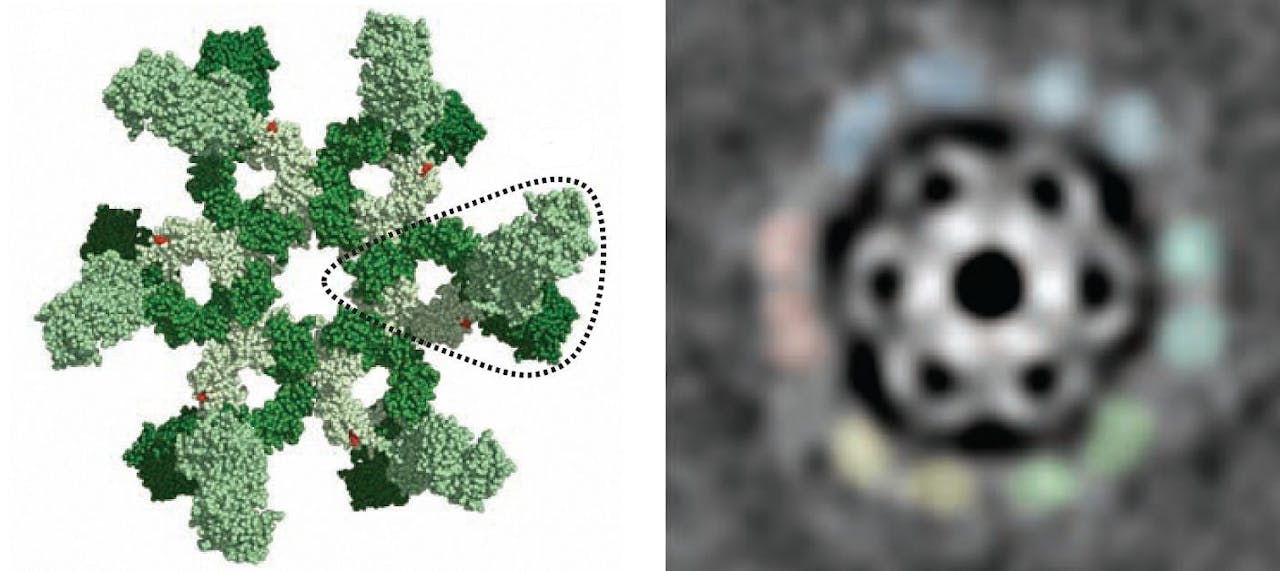
In Science beschrijven de onderzoekers hoe de antilichamen zich organiseren tijdens de interactie met de kankercel. Ze ontdekten dat een cluster van zes antilichamen bepalend is voor de activering van de opruimdienst. Zo’n hexameer zorgt voor een optimale binding van de eerste component van het complementsysteem (dat de toepasselijke naam ‘C1 molecuul’ draagt).
Het hexameer fungeert als een soort ‘docking station’ voor het C1 molecuul. Is dat eenmaal netjes gebonden, dan kan een vernietigende kettingreactie volgen. Uiteindelijk raakt daarbij het membraan van de kankercel doorboord en de cel sterft. De boom is om, opgeruimd staat netjes.
Nieuwe medicijnen
De fundamentele inzichten in de moleculaire opbouw van het docking station zijn inmiddels al zeer nuttig gebleken. De onderzoekers wisten in het lab de activerende werking van antilichamen te versterken of verzwakken via kleine veranderingen in hun aminozuren. Onderzoeksleider Paul Parren van Genmab: “Dit onderzoek biedt waardevolle aanknopingspunten om bestaande therapeutische antilichamen te verbeteren en hele nieuwe varianten te maken.”
Voor Parren is het onderzoek is een mooi voorbeeld van waardevolle samenwerking tussen universiteiten en industrie: “Je moet eerst fundamentele biologische vragen oplossen voordat je echt effectieve medicijnen kunt ontwikkelen. Dat is precies wat we hier gedaan hebben.”