Eiwitten zijn onmisbaar voor de processen in een levende cel, maar ze zijn alleen nuttig als ze op de juiste manier zijn gevouwen. Die complexe vorm van natuurlijke eiwitten is gaandeweg door evolutie ontstaan. Inmiddels kunnen wetenschappers ook eiwitten gericht aanpassen om zo de gevouwen structuur te veranderen. Maar nu blijkt er nog een derde mogelijkheid te bestaan. Groningse chemici hebben ontdekt dat eenvoudige bouwstenen ook spontaan complexe, gevouwen moleculen kunnen vormen.
Een levende cel is een buitengewoon ingewikkeld geheel waarin heel veel processen tegelijkertijd plaatsvinden. Om te zorgen dat al die verschillende taken op het juiste moment en op de juiste plaats worden uitgevoerd zijn eiwitten nodig. Eiwitten zijn heel grote moleculen die je kunt zien als een lange snoer van ‘kralen’, de zogeheten aminozuren, die in precies de juiste volgorde aan elkaar zijn verbonden. Maar zo’n snoer kan nog niks. Voordat een eiwit zijn taak kan uitvoeren, moet het snoer op precies de juiste manier worden opgevouwen. Hierdoor ontstaat een complexe, driedimensionale structuur.
We weten inmiddels behoorlijk goed hoe in een moderne cel een eiwit z’n uiteindelijke opgevouwen vorm krijgt, maar daarvoor zijn weer allerlei andere ingewikkelde moleculen en processen nodig die ook gedurende de evolutie zijn ontstaan. Maar voor het allereerste leven dat miljarden jaren geleden is ontstaan, moet het veel eenvoudiger zijn geweest. De onderzoeksgroep van Sijbren Otto, hoogleraar systeemchemie aan de Rijksuniversiteit Groningen, bestudeert hoe uit eenvoudige kleine moleculen, grotere en meer ingewikkelde structuren kunnen ontstaan zonder dat er een levende cel bij betrokken is. Je kunt dat zien als ‘chemische evolutie’.
De groep van Otto kijkt onder meer naar de vorming van ringvormige structuren uit kleinere eenheden. In eerder onderzoek hebben ze laten zien dat die ringen op hun beurt weer stapeltjes vormen die kunnen groeien en delen. Daarbij vertonen ze een vorm van chemische evolutie, er ontstaan gaandeweg onverwachte, nieuwe samenstellingen in de stapeltjes.
Maar in een nieuw experiment gebeurde er onlangs iets anders. Otto: “Een van mijn promovendi, Bin Liu, zag dat zich heel grote ringen vormden, polymeren (langgerekte moleculen met herhalende bouwstenen, red.) die bestaan uit vijftien bouwstenen.” Die ringen waren zeer stabiel, zodat bijna alle bouwstenen uiteindelijk in de ringen eindigden.
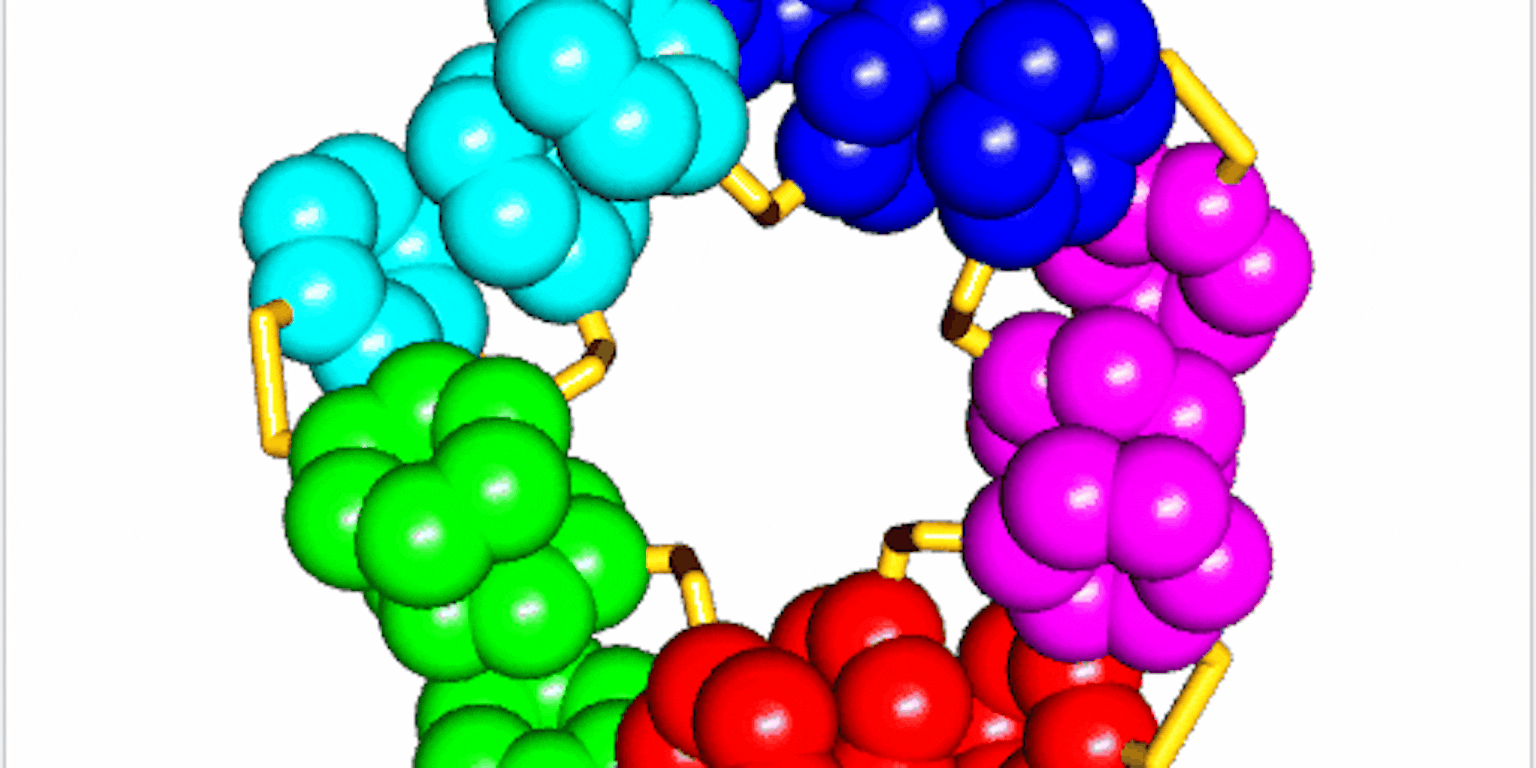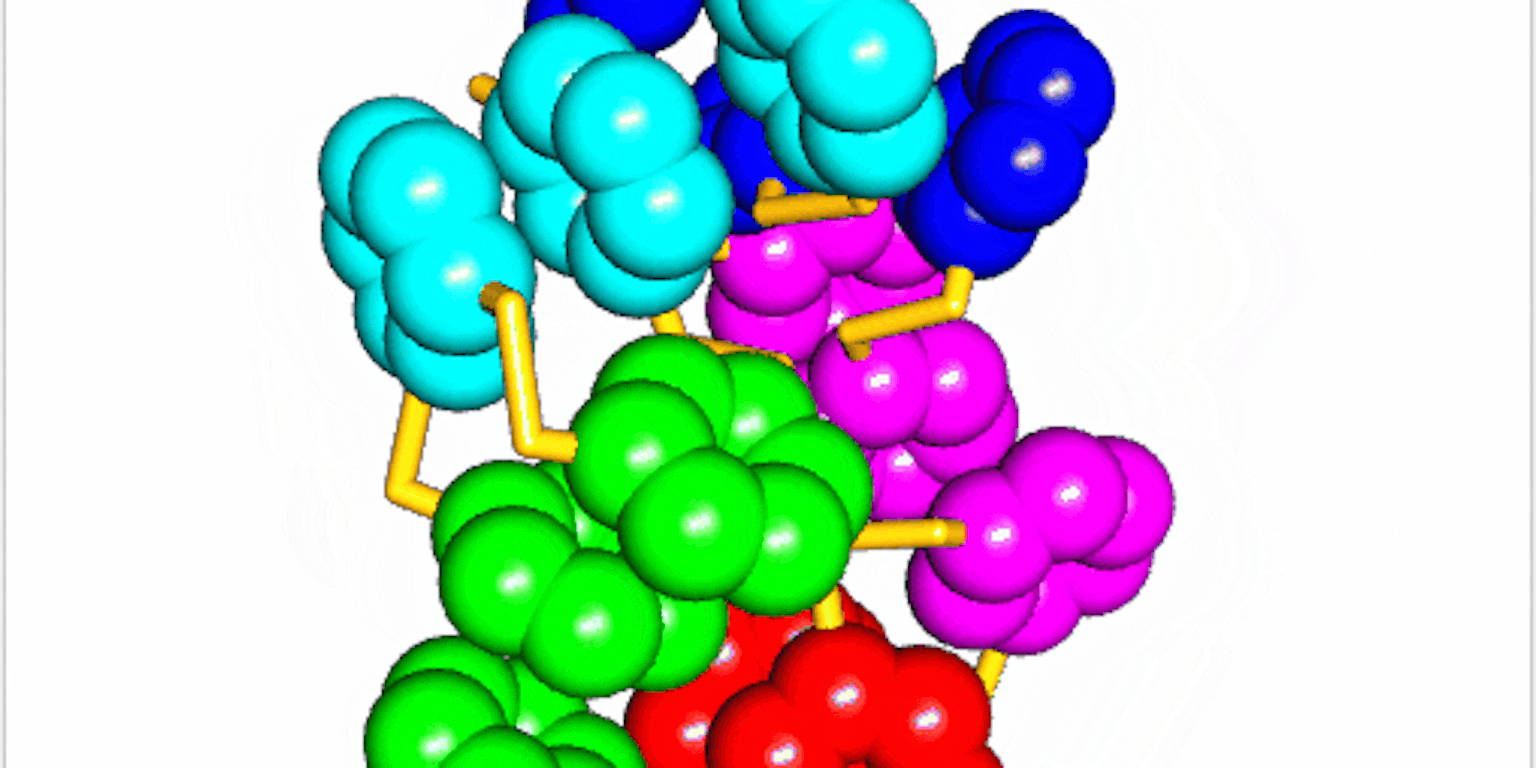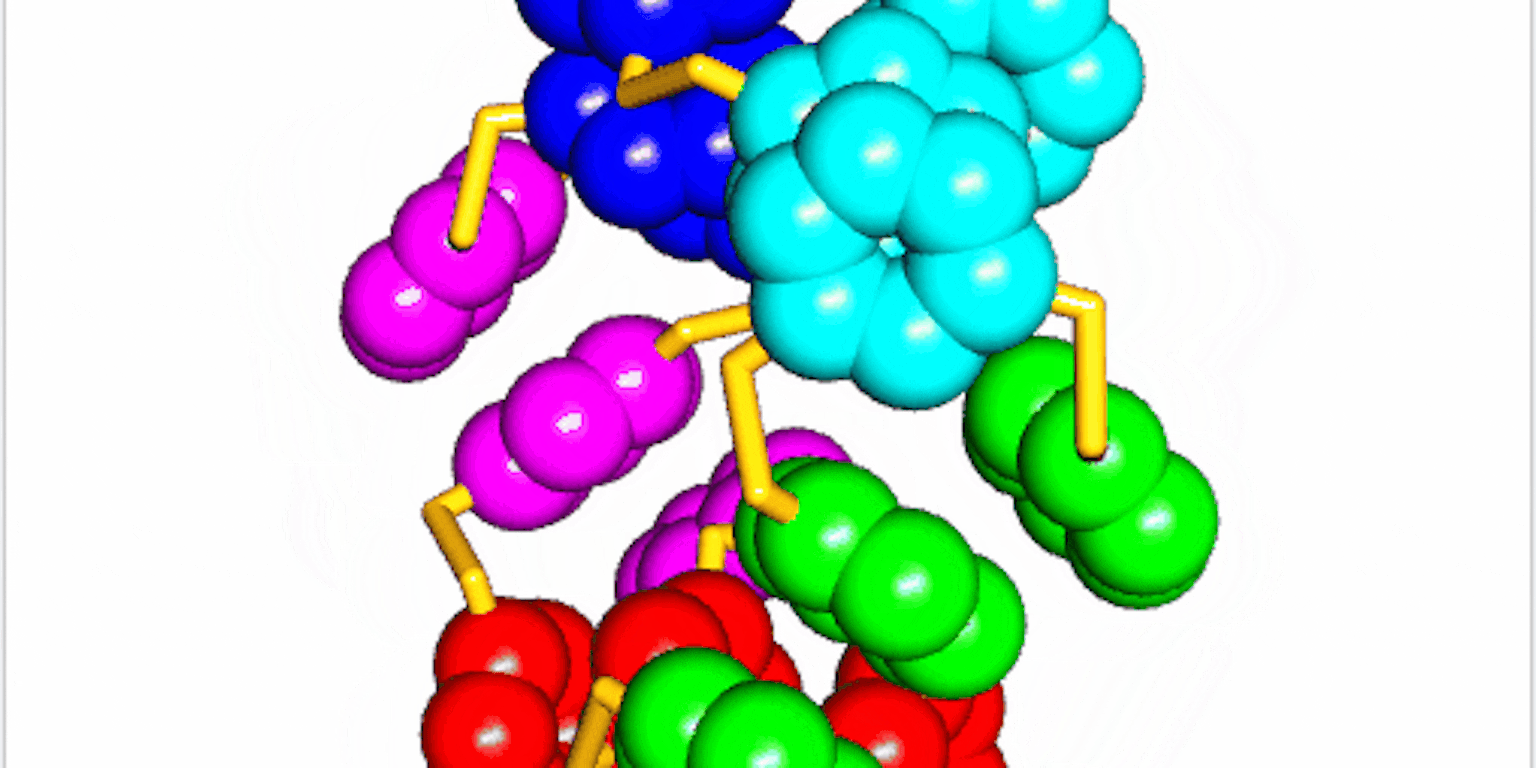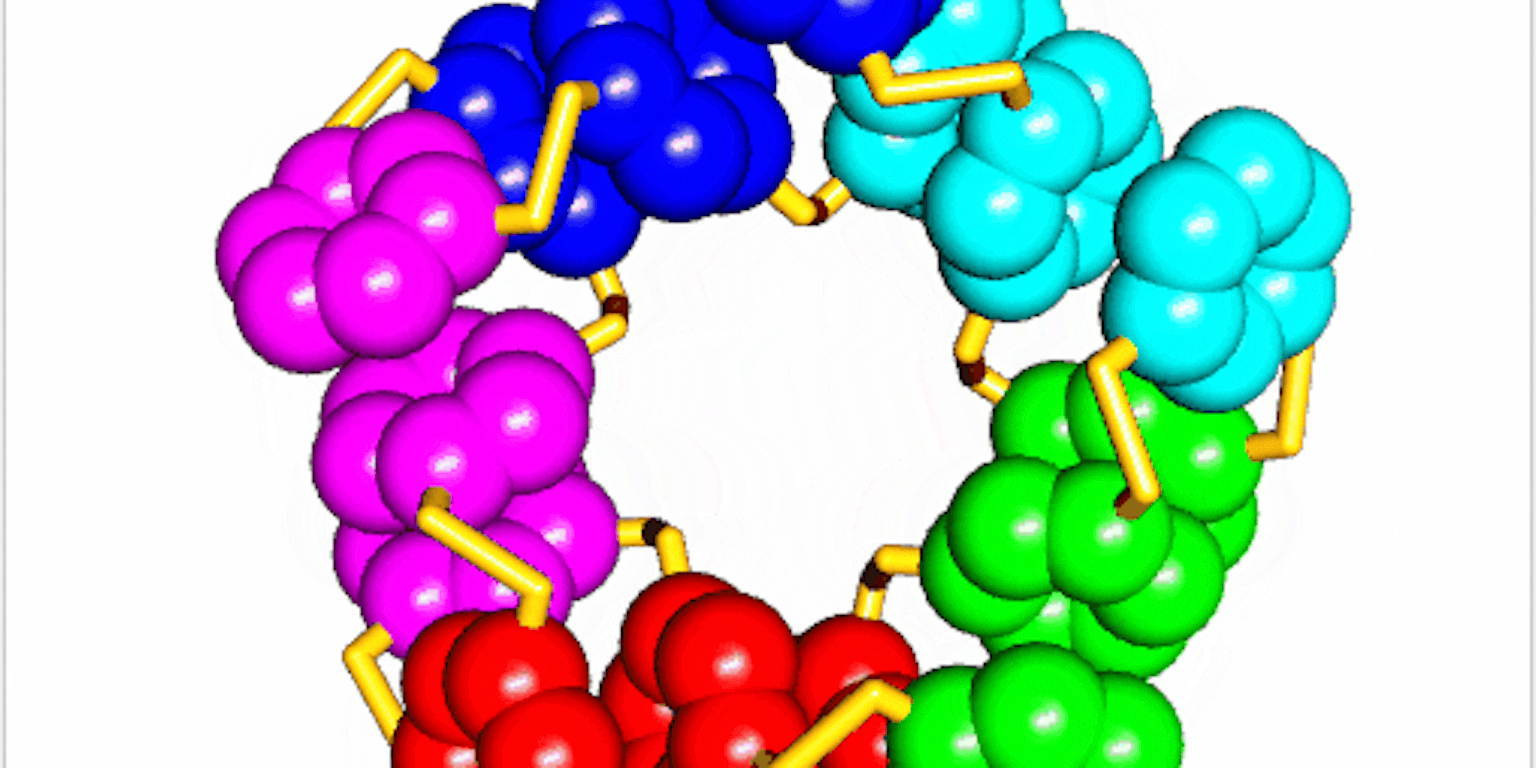
Na bestudering van de structuur van de ringen bleek dat ze ook nog eens gevouwen waren.
Naar het midden
“Als ringen stapeltjes vormen trekken de verschillende ringen elkaar aan. In dit geval was er een interactie tussen stukjes binnen de grotere ring zelf.” De waterafstotende delen van de ring vouwden zich naar het midden van het molecuul, iets dat ook gebeurt bij eiwitten in water. Maar de manier van vouwen van de ringen is totaal anders dan bij eiwitten. “In onze moleculen zitten de bouwstenen aan elkaar vast via een disulfide binding [binding tussen twee zwavelatomen, red.]. Dit verschil zorgt voor een ander vouwpatroon.”
Het is de eerste beschrijving van een complexe gevouwen structuur, een zogeheten foldameer (van het Engelse fold, vouwen) die radicaal afwijkt van eiwitten. “Ondanks tientallen jaren onderzoek hebben we nog steeds geen betrouwbare ontwerpregels waarmee we de vouwing van eiwitten helemaal kunnen voorspellen”, legt Otto uit. Dit remt de ontwikkeling van nieuwe, in het lab ontworpen enzymen. Dat zijn speciale eiwitten die reacties versnellen, het zijn katalysatoren. Een nieuwe klasse van zelf-vouwende moleculen kan helpen om te begrijpen welke regels er gelden bij het vouwen van moleculen. “Het molecuul dat we in ons artikel beschrijven is bovendien de eerste van een serie die we inmiddels hebben ontdekt, en die we in vervolgartikelen zullen beschrijven.”
Kurkentrekker
Eiwitten kennen twee belangrijke onderdelen in de gevouwen structuren: de alfa helix en de bèta sheet. De alfa helix is een spiraal, zoals een kurkentrekker. De bèta sheet is een plat vlak. “Bij het ontwerpen van eiwitten gebruiken wetenschappers variaties op deze thema’s, door bijvoorbeeld een extra helix toe te voegen”, zegt Otto. “Ze blijven daardoor dicht bij wat de natuur hen aanbiedt.” De nieuw ontdekte gevouwen structuur levert vijf groepen van elk vijf gestapelde ringen op. Het hele molecuul heeft daardoor een vijfzijdige symmetrie. “Maar de andere gevouwen structuren die we nog bestuderen laten weer andere soorten vouwing zien.”
De ontdekking van nieuwe, gevouwen moleculen leidt tot een belangrijke conclusie: complexiteit kan spontaan ontstaan. “Dit is interessant voor onderzoek naar het ontstaan van leven. Blijkbaar kun je dit soort complexe moleculen krijgen voordat er sprake is van biologische evolutie.” Vouwing is zelfs de drijvende kracht achter de vorming van het nieuwe molecuul, legt Otto uit. “Dat is heel bijzonder. Het energieniveau van dit molecuul is erg laag, waardoor het evenwicht van een willekeurig mengsel van kleinere ringen verschuift naar deze zeer stabiele polymeer van vijftien bouwstenen.”
De nieuwe ontdekking zal het begrip van gevouwen moleculen vergroten, wat kan leiden tot gericht ontwerp van functionele moleculen.
Of de nu ontdekte polymeren op basis van een disulfide verbinding ook werken als katalysatoren, net als natuurlijke enzymen, is nog niet duidelijk. “We weten dat ze andere moleculen kunnen binden, maar we onderzoeken nog of ze ook in staat zijn tot katalyse.” Vouwen is belangrijk om enzymen een zogeheten actief centrum te geven, de plek waar de chemische reactie plaatsvindt. “Je moet daarvoor delen van het molecuul heel precies ten opzichte van elkaar positioneren. Dit kan niet via directe chemische bindingen tussen aminozuren, het lukt alleen via vouwen.”